HOME>実験紹介>家庭向け>EH007 クエン酸レモネード
レモン汁の酸味はクエン酸によるものです。酸の強さを、中和に使った重曹の量で測ることで、レモン汁に含まれるクエン酸の量を知ることができます。
レモン汁で作ったレモネードと、クエン酸で作ったレモネード、同じ味になるでしょうか?
レモネードの酸味は胃腸に負荷をかけます(特に空腹時)。飲み過ぎに注意しましょう。
使用器具および試薬
使用器具
・深めのコップ
・計量カップ
・キッチンスケール
使用試薬
・重曹
・クエン酸(食用)
・レモン汁
実験方法
1.

計量カップにレモン汁を大さじ 2入れて、水を追加して 100 mLになるようにする。よく混ぜたらコップに移す
2.

重曹を 1 gずつ(または0.5gずつ)入れていき、重曹を入れても泡が出なくなったら終了。最後に入れた重曹の分を除いて、今まで入れた重曹の量をメモする。
3.

空のコップを5つ用意し、それぞれのコップにクエン酸を1g、2g、3g、4g、5g入れて、水を100 mL追加して溶かす。
4.

それぞれのクエン酸水に手順2と同じ方法を行う。
5.
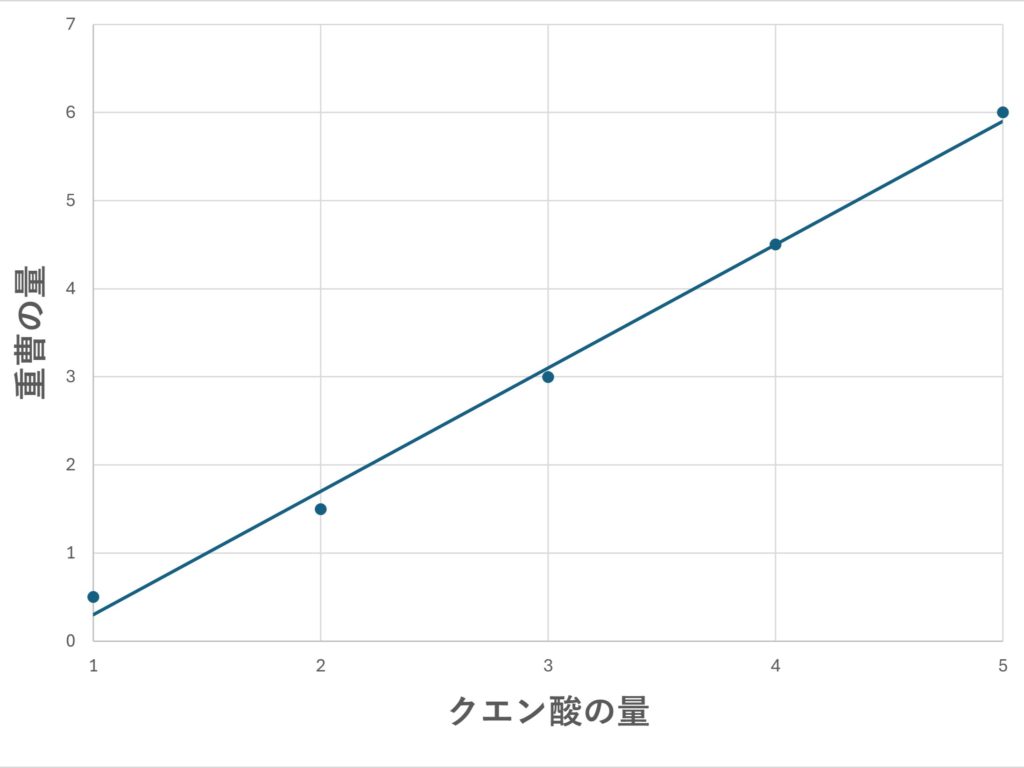
横軸をクエン酸の重さ、縦軸をメモした重曹の量としたグラフを作る。その後②でメモした重曹の量に対応するクエン酸の量を、グラフから求める。
6.

手順1のレモン水をもう一度作り、別のコップに100 mLの水に手順5で求めたクエン酸の量溶かする。2つを味見して、すっぱさや風味を比べてみる。(お好みで砂糖もしくはガムシロップを同量ずつ加えてもOK。)
後片付け
実験後の液体は全て流しに捨てましょう
ポイント
実験方法②と④では、粉の追加→かき混ぜるなどして発泡がおさまるのを待つ→粉を追加→…… というふうに繰り返していき、粉を入れても泡が出なくなったらやめます。
重曹はレモン汁の酸成分(H+)に反応すると、二酸化炭素を放出します。泡が出るのはこのためです。
NaHCO3+H+→Na++CO2+H2O
酸性、アルカリ性の強さを数値で表す「pH」は、水に含まれるH+の量によってその数値が変わります。ちょっとややこしいですが、H+が多いほどpHは0(強酸性)に近づき、逆に少ないほど14(強アルカリ性)に近づきます。レモンは一般的にpH=2です。強い酸性ですね。
先ほどの化学反応式のように、重曹がH+を消費して二酸化炭素を作ると、その分H+の量は少なくなるので、pHは大きくなる。つまりアルカリ性に近づいていきます。
またレモン汁に含まれるクエン酸は、分子一個あたりH+を3つ出します。つまり重曹はクエン酸1分子に反応すると二酸化炭素3つ作り出すことになりますね。※ただし、3つのH+が同時に消費されることはないことには注意
重曹をレモン水/クエン酸水に入れていくと、ある時点で泡が出なくなります。この時中和が完了したことになるので、pHも中性付近になります。
この方法以外でも酸性の強さを測る方法はいくつかあります。より正確な方法をはあるでしょうか?探ってみましょう。

